Лютецій— рідкісний рідкоземельний елемент з високою ціною, мінімальними запасами та обмеженим використанням. Він м’який та розчинний у розведених кислотах і може повільно реагувати з водою.
Природні ізотопи включають 175Lu та період напіврозпаду 2,1 × 10 ^ 10 років. β-випромінювач 176Lu. Його отримують шляхом відновлення фториду лютецію(III) LuF∨·2H₂O кальцієм.
Основне застосування — як каталізатор для реакцій крекінгу нафти, алкілування, гідрування та полімеризації; крім того, танталат лютецію також може бути використаний як матеріал для порошку рентгенівської флуоресценції; 177Lu, радіонуклід, може бути використаний для променевої терапії пухлин.

Відкриття історії
Відкрив: Г. Урбан
Відкритий у 1907 році
Лютецій був виділений з ітербію французьким хіміком Ульбаном у 1907 році, і він також був рідкісноземельним елементом, відкритим та підтвердженим на початку 20 століття. Латинська назва лютецію походить від давньої назви Парижа, Франція, який є батьківщиною Урбана. Відкриття лютецію та ще одного рідкісноземельного елемента європію завершило відкриття всіх рідкісноземельних елементів, присутніх у природі. Їх відкриття можна розглядати як відкриття четвертих воріт до відкриття рідкісноземельних елементів та завершення четвертого етапу відкриття рідкісноземельних елементів.
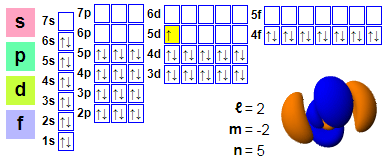
Електронна конфігурація
Електронні домовленості:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d1
Лютецій — сріблясто-білий метал, найтвердіший і найщільніший серед рідкоземельних елементів; температура плавлення 1663 ℃, температура кипіння 3395 ℃, густина 9,8404. Лютецій відносно стійкий на повітрі; оксид лютецію — безбарвний кристал, який розчиняється в кислотах з утворенням відповідних безбарвних солей.
Блиск лютецію, що є рідкоземельним металом, знаходиться між сріблом і залізом. Вміст домішок суттєво впливає на їхні властивості, тому в літературі часто зустрічаються суттєві відмінності в їхніх фізичних властивостях.
Металі ітрій, гадоліній та лютецій мають сильну корозійну стійкість і можуть довго зберігати свій металевий блиск.
Застосування
Через труднощі з виробництвом та високі ціни лютецій має мало комерційного застосування. Властивості лютецію суттєво не відрізняються від інших лантаноїдів, але його запаси відносно менші, тому в багатьох місцях для заміни лютецію зазвичай використовуються інші лантаноїди.
Лютецій можна використовувати для виготовлення деяких спеціальних сплавів, таких як алюмінієвий сплав лютецію, який можна використовувати для нейтронно-активаційного аналізу. Лютецій також можна використовувати як каталізатор для реакцій крекінгу нафти, алкілування, гідрування та полімеризації. Крім того, легування лютецію в деяких лазерних кристалах, таких як ітрій-алюмінієвий гранат, може покращити його лазерні характеристики та оптичну однорідність. Крім того, лютецій також можна використовувати для люмінофорів: танталат лютецію є найкомпактнішим білим матеріалом, відомим на даний момент, і є ідеальним матеріалом для рентгенівських люмінофорів.
177Lu – це синтетичний радіонуклід, який може бути використаний для променевої терапії пухлин.
Оксид лютеціюлегований церій ітрій лютецій силікат кристал
Час публікації: 26 червня 2023 р.