SкандіюСкандій, з символом елемента Sc та атомним номером 21, легко розчинний у воді, може взаємодіяти з гарячою водою та легко темніє на повітрі. Його головна валентність дорівнює +3. Його часто змішують з гадолінієм, ербієм та іншими елементами, з низьким виходом та вмістом приблизно 0,0005% у земній корі. Скандій часто використовується для виготовлення спеціального скла та легких жароміцних сплавів.
Наразі підтверджені запаси скандію у світі становлять лише 2 мільйони тонн, 90~95% яких міститься в бокситах, фосфоритах та залізо-титанових рудах, а невелика частина - в уранових, торієвих, вольфрамових та рідкісноземельних рудах, в основному поширених у Росії, Китаї, Таджикистані, Мадагаскарі, Норвегії та інших країнах. Китай дуже багатий на ресурси скандію, маючи величезні мінеральні запаси, пов'язані зі скандієм. За неповною статистикою, запаси скандію в Китаї становлять близько 600 000 тонн, які містяться в родовищах бокситів та фосфоритів, порфірових та кварцово-жильних вольфрамових родовищах у Південному Китаї, родовищах рідкісноземельних металів у Південному Китаї, родовищі рідкісноземельних залізних руд Баян Обо у Внутрішній Монголії та родовищі ванадій-титан-магнетиту Паньчжихуа у провінції Сичуань.
Через дефіцит скандію ціна на нього також дуже висока, і на своєму піку ціна на скандій зросла в 10 разів порівняно з ціною на золото. Хоча ціна на скандій впала, вона все ще в чотири рази перевищує ціну на золото!
Відкриття історії
У 1869 році Менделєєв помітив розрив в атомній масі між кальцієм (40) і титаном (48) і передбачив, що тут також існує невідкритий елемент із проміжною атомною масою. Він передбачив, що його оксидом є X ₂ O Å. Скандій був відкритий у 1879 році Ларсом Фредеріком Нільсоном з Уппсальського університету у Швеції. Він видобув його з чорного рідкісного золотого рудника, складної руди, що містить 8 типів оксидів металів. Він видобувОксид ербію(III)з чорної рідкісної золотої руди та отриманоїОксид ітербію(III)з цього оксиду, і є інший оксид легшого елемента, спектр якого показує, що це невідомий метал. Це метал, передбачений Менделєєвим, оксид якого єSc₂O₃Сам металевий скандій був отриманий зХлорид скандіюшляхом електролітичного плавлення в 1937 році.
Менделєєв
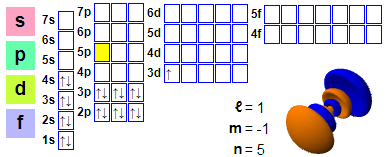
Електронна конфігурація
Електронна конфігурація: 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Скандій — м’який сріблясто-білий перехідний метал з температурою плавлення 1541 ℃ та температурою кипіння 2831 ℃.
Протягом значного періоду часу після його відкриття використання скандію не було продемонстровано через складність його виробництва. Зі зростаючим удосконаленням методів розділення рідкоземельних елементів зараз існує зрілий технологічний процес очищення сполук скандію. Оскільки скандій менш лужний, ніж ітрій та лантаноїди, гідроксид є найслабшим, тому змішаний мінерал рідкоземельних елементів, що містить скандій, буде відокремлений від рідкоземельного елемента методом «ступінчастого осадження», коли гідроксид скандію(III) обробляють аміаком після переведення в розчин. Інший метод полягає у відділенні нітрату скандію шляхом полярного розкладання нітрату. Оскільки нітрат скандію найлегше розкладається, скандій можна відокремити. Крім того, важливим джерелом скандію також є комплексне вилучення супутнього скандію з родовищ урану, торію, вольфраму, олова та інших корисних копалин.
Після отримання чистої сполуки скандію її перетворюють на ScCl Å та плавлять разом з KCl та LiCl. Розплавлений цинк використовується як катод для електролізу, що призводить до осадження скандію на цинковому електроді. Потім цинк випаровують, отримуючи металевий скандій. Це легкий сріблясто-білий метал з дуже активними хімічними властивостями, який може реагувати з гарячою водою, утворюючи водень. Тому металевий скандій, який ви бачите на зображенні, герметично поміщений у пляшку та захищений аргоном, інакше скандій швидко утворить темно-жовтий або сірий оксидний шар, втрачаючи свій блискучий металевий блиск.
Застосування
Освітлювальна промисловість
Використання скандію зосереджено в дуже яскравих напрямках, і не буде перебільшенням назвати його Сином Світла. Перша чарівна зброя скандію називається скандієво-натрієва лампа, яку можна використовувати для освітлення тисяч домогосподарств. Це металогалогенна електрична лампа: колба наповнена йодидом натрію та трийодидом скандію, а скандієва та натрієва фольга додаються одночасно. Під час високовольтного розряду іони скандію та іони натрію відповідно випромінюють світло з характерними довжинами хвиль випромінювання. Спектральні лінії натрію мають 589,0 та 589,6 нм, два відомих жовтих світла, тоді як спектральні лінії скандію мають 361,3~424,7 нм, серію випромінювань ближнього ультрафіолетового та синього світла. Оскільки вони доповнюють один одного, загальний колір світла, що виробляється, є білим. Саме тому, що скандієво-натрієві лампи мають такі характеристики, як висока світлова ефективність, гарний колір світла, енергозбереження, тривалий термін служби та сильна здатність розсіювати туман, вони можуть широко використовуватися для телевізійних камер, освітлення площ, спортивних майданчиків та доріг, і відомі як джерела світла третього покоління. У Китаї цей тип ламп поступово просувається як нова технологія, тоді як у деяких розвинених країнах цей тип ламп широко використовувався ще на початку 1980-х років.
Другою чарівною зброєю скандію є сонячні фотоелектричні елементи, які можуть збирати світло, розсіяне на землі, та перетворювати його на електрику для живлення людського суспільства. Скандій є найкращим бар'єрним металом у металоізоляторах, напівпровідникових кремнієвих сонячних елементах та сонячних батареях.
Його третя магічна зброя називається джерелом γ-A-променів. Ця магічна зброя може яскраво світити сама по собі, але такий вид світла неможливо сприйняти неозброєним оком, це потік фотонів високої енергії. Зазвичай ми видобуваємо 45Sc з мінералів, який є єдиним природним ізотопом скандію. Кожне ядро 45Sc містить 21 протон і 24 нейтрони. 46Sc, штучний радіоактивний ізотоп, може використовуватися як джерело γ-випромінювання або як трасерні атоми, які також можуть бути використані для променевої терапії злоякісних пухлин. Існують також такі застосування, як ітрій-галій-скандій-гранатовий лазер.Фторид скандіюСкляне інфрачервоне оптичне волокно та електронно-променева трубка зі скандієвим покриттям на телебаченні. Здається, що скандій народжується з яскравістю.
Промисловість сплавів
Скандій у своїй елементарній формі широко використовується для легування алюмінієвих сплавів. Якщо до алюмінію додати кілька тисячних часток скандію, утвориться нова фаза Al3Sc, яка відіграватиме роль метаморфізму в алюмінієвому сплаві та значно змінить структуру та властивості сплаву. Додавання 0,2%~0,4% Sc (що дійсно схоже на пропорцію додавання солі до смажених овочів вдома, потрібна лише невелика кількість) може підвищити температуру рекристалізації сплаву на 150-200 ℃ та значно покращити міцність за високих температур, структурну стабільність, зварювальні характеристики та корозійну стійкість. Це також може уникнути явища окрихчення, яке легко виникає під час тривалої роботи за високих температур. Високоміцні та високоміцні алюмінієві сплави, нові високоміцні корозійностійкі зварювані алюмінієві сплави, нові високотемпературні алюмінієві сплави, високоміцні алюмінієві сплави, стійкі до нейтронного опромінення тощо, мають дуже привабливі перспективи розвитку в аерокосмічній галузі, авіації, кораблях, ядерних реакторах, легких транспортних засобах та швидкісних поїздах.
Скандій також є чудовим модифікатором заліза, а невелика кількість скандію може значно покращити міцність і твердість чавуну. Крім того, скандій також можна використовувати як добавку для високотемпературних вольфрамових та хромових сплавів. Звичайно, окрім виготовлення весільного одягу, скандій має високу температуру плавлення та щільність, подібну до алюмінію, і також використовується у легких сплавах з високою температурою плавлення, таких як титановий сплав скандію та магнієвий сплав скандію. Однак через високу ціну він зазвичай використовується лише у високотехнологічних галузях виробництва, таких як космічні човники та ракети.
Керамічний матеріал
Скандій, єдина речовина, зазвичай використовується в сплавах, і його оксиди відіграють важливу роль у керамічних матеріалах подібним чином. Тетрагональний керамічний матеріал на основі діоксиду цирконію, який можна використовувати як електродний матеріал для твердооксидних паливних елементів, має унікальну властивість, за якої провідність цього електроліту зростає зі збільшенням температури та концентрації кисню в навколишньому середовищі. Однак кристалічна структура цього керамічного матеріалу сама по собі не може існувати стабільно і не має промислової цінності; для збереження її початкових властивостей необхідне легування деякими речовинами, які можуть зафіксувати цю структуру. Додавання 6~10% оксиду скандію створює подібну бетонну структуру, завдяки чому діоксид цирконію можна стабілізувати на квадратній решітці.
Також існують інженерні керамічні матеріали, такі як високоміцний та стійкий до високих температур нітрид кремнію, як ущільнювачі та стабілізатори.
Як ущільнювач,Оксид скандіюможе утворювати тугоплавку фазу Sc2Si2O7 на краю дрібних частинок, тим самим зменшуючи високотемпературну деформацію інженерної кераміки. Порівняно з іншими оксидами, він може краще покращувати високотемпературні механічні властивості нітриду кремнію.
Каталітична хімія
У хімічній інженерії скандій часто використовується як каталізатор, тоді як Sc2O3 може бути використаний для дегідратації та розкислення етанолу або ізопропанолу, розкладання оцтової кислоти та виробництва етилену з CO та H2. Каталізатор PtAl, що містить Sc2O3, також є важливим каталізатором для процесів гідрогенізації, очищення та переробки важкої нафти в нафтохімічній промисловості. У реакціях каталітичного крекінгу, таких як кумол, активність цеолітного каталізатора Sc-Y у 1000 разів вища, ніж у алюмосилікатного каталізатора; порівняно з деякими традиційними каталізаторами, перспективи розвитку скандієвих каталізаторів будуть дуже яскравими.
Атомна енергетика
Додавання невеликої кількості Sc2O3 до UO2 у високотемпературному ядерному паливі реактора може запобігти перетворенню кристалічної решітки, збільшенню об'єму та розтріскуванню, спричиненим перетворенням UO2 в U3O8.
Паливний елемент
Аналогічно, додавання від 2,5% до 25% скандію до нікель-лужних акумуляторів збільшить термін їхньої служби.
Сільськогосподарська селекція
У сільському господарстві насіння, таке як кукурудза, буряк, горох, пшениця та соняшник, можна обробляти сульфатом скандію (концентрація зазвичай становить 10⁻³~10⁻⁶ моль/л, різні рослини мають різну концентрацію), і фактичний ефект сприяння проростанню вже досягнутий. Через 8 годин суха маса коренів та бруньок збільшилася на 37% та 78% відповідно порівняно з розсадою, але механізм цього процесу все ще вивчається.
Відтоді, як Нільсен звернув увагу на дані про атомну масу, скандій з'явився в полі зору людей лише сто чи двадцять років тому, але він майже сто років лежав на лаві. Лише бурхливий розвиток матеріалознавства наприкінці минулого століття приніс йому життєву силу. Сьогодні рідкоземельні елементи, включаючи скандій, стали гарячими зірками в матеріалознавстві, відіграючи постійно мінливу роль у тисячах систем, щодня приносячи більше зручностей у наше життя та створюючи економічну цінність, яку ще важче виміряти.
Час публікації: 29 червня 2023 р.