Європіум, символ — Eu, а атомний номер — 63. Як типовий представник лантаноїдів, європій зазвичай має валентність +3, але також поширена валентність кисню +2. Існує менше сполук європію з валентним станом +2. Порівняно з іншими важкими металами, європій не має значних біологічних ефектів і є відносно нетоксичним. Більшість застосувань європію використовують ефект фосфоресценції сполук європію. Європій є одним з найменш поширених елементів у Всесвіті; у Всесвіті лише близько 5 × 10⁻⁶% речовини становить європій.
Європій присутній у монациті
Відкриття європію
Історія починається наприкінці 19 століття: у той час чудові вчені почали систематично заповнювати прогалини, що залишилися, в періодичній таблиці Менделєєва, аналізуючи спектр атомного випромінювання. На сьогоднішній погляд, ця робота не є складною, і студент може її виконати; але в той час у вчених були лише прилади з низькою точністю та зразки, які було важко очистити. Тому протягом усієї історії відкриття лантаноїдів усі «квазі»-відкривачі продовжували робити неправдиві заяви та сперечатися один з одним.
У 1885 році сер Вільям Крукс відкрив перший, але не дуже чіткий сигнал елемента 63: він спостерігав специфічну червону спектральну лінію (609 нм) у зразку самарію. Між 1892 і 1893 роками першовідкривач галію, самарію та диспрозію Поль еміль Лекок де Буабодран підтвердив цю смугу та відкрив ще одну зелену смугу (535 нм).
Далі, у 1896 році, Егєн Анатоль Демар терпляче виділив оксид самарію та підтвердив відкриття нового рідкоземельного елемента, розташованого між самарієм та гадолінієм. Він успішно виділив цей елемент у 1901 році, що ознаменувало завершення шляху відкриття: «Я сподіваюся назвати цей новий елемент європієм, з символом Eu та атомною масою близько 151».
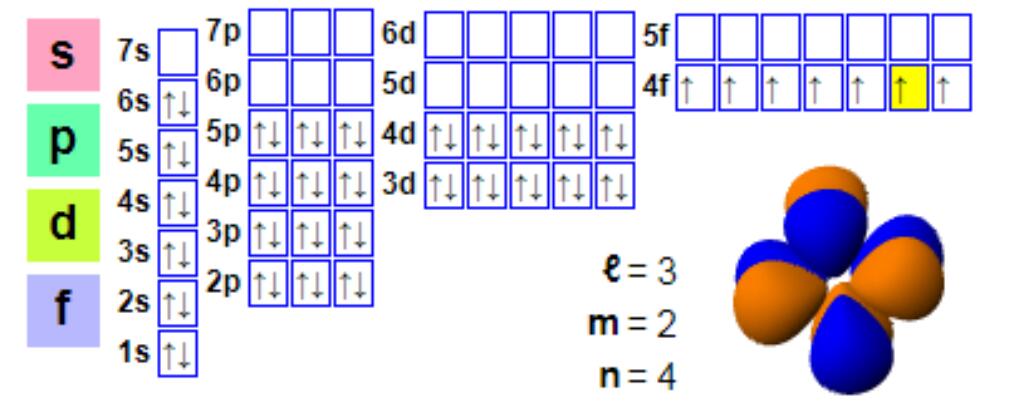
Електронна конфігурація
Електронна конфігурація:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Хоча європій зазвичай тривалентний, він схильний до утворення двовалентних сполук. Це явище відрізняється від утворення сполук з валентністю +3 більшістю лантаноїдів. Двовалентний європій має електронну конфігурацію 4f7, оскільки напівзаповнена f-оболонка забезпечує більшу стабільність, а європій (II) та барій (II) подібні. Двовалентний європій є м'яким відновником, який окислюється на повітрі, утворюючи сполуку європію (III). В анаеробних умовах, особливо в умовах нагрівання, двовалентний європій є достатньо стабільним і має тенденцію до включення до кальцію та інших лужноземельних мінералів. Цей процес іонного обміну є основою «негативної аномалії європію», тобто, порівняно з великою кількістю хондриту, багато лантаноїдних мінералів, таких як монацит, мають низький вміст європію. Порівняно з монацитом, бастнезит часто демонструє менше негативних аномалій європію, тому бастнезит також є основним джерелом європію.
Європій — це залізистосірий метал з температурою плавлення 822 °C, температурою кипіння 1597 °C та густиною 5,2434 г/см³; це найменш щільний, найм'якший та найлеткіший елемент серед рідкоземельних елементів. Європій — найактивніший метал серед рідкоземельних елементів: за кімнатної температури він миттєво втрачає свій металевий блиск на повітрі та швидко окислюється на порошок; бурхливо реагує з холодною водою з утворенням водню; Європій може реагувати з бором, вуглецем, сіркою, фосфором, воднем, азотом тощо.
Застосування європію
Сульфат європію випромінює червону флуоресценцію під ультрафіолетовим світлом
Жорж Урбен, молодий видатний хімік, успадкував спектроскопічний прилад Демарея та виявив, що зразок оксиду ітрію(III), легований європієм, випромінював дуже яскраве червоне світло у 1906 році. Це початок довгої подорожі фосфоресцентних матеріалів європію, які використовувалися не лише для випромінювання червоного, а й синього світла, оскільки спектр випромінювання Eu2+ потрапляє в цей діапазон.
Люмінофор, що складається з червоних випромінювачів Eu3+, зелених Tb3+ та синіх Eu2+, або їх комбінації, може перетворювати ультрафіолетове світло на видиме. Ці матеріали відіграють важливу роль у різних приладах по всьому світу: екранах, що підсилюють рентгенівське випромінювання, електронно-променевих трубках або плазмових екранах, а також у новітніх енергозберігаючих люмінесцентних лампах та світлодіодах.
Флуоресцентний ефект тривалентного європію також може бути сенсибілізований органічними ароматичними молекулами, і такі комплекси можуть бути застосовані в різних ситуаціях, що вимагають високої чутливості, таких як чорнила для боротьби з підробками та штрих-коди.
З 1980-х років європій відіграє провідну роль у високочутливому біофармацевтичному аналізі з використанням методу холодної флуоресценції з роздільною здатністю в часі. У більшості лікарень та медичних лабораторій такий аналіз став рутинною справою. У дослідженнях у галузі біології, включаючи біологічну візуалізацію, флуоресцентні біологічні зонди, виготовлені з європію та інших лантаноїдів, є повсюдними. На щастя, одного кілограма європію достатньо для проведення приблизно одного мільярда аналізів – після того, як уряд Китаю нещодавно обмежив експорт рідкісноземельних елементів, промислово розвинені країни, стурбовані дефіцитом сховищ рідкісноземельних елементів, не повинні турбуватися про подібні загрози для таких застосувань.
Оксид європію використовується як люмінофор для стимульованого випромінювання в новій рентгенівській медичній діагностичній системі. Оксид європію також може бути використаний для виготовлення кольорових лінз та оптоелектронних фільтрів, для магнітних накопичувачів пухирців, а також у контрольних матеріалах, захисних матеріалах та конструкційних матеріалах атомних реакторів. Оскільки його атоми можуть поглинати більше нейтронів, ніж будь-який інший елемент, його зазвичай використовують як матеріал для поглинання нейтронів в атомних реакторах.
У сучасному світі, що швидко розвивається, нещодавно виявлене застосування європію може мати глибокий вплив на сільське господарство. Вчені виявили, що пластмаси, леговані двовалентним європієм та одновалентною міддю, можуть ефективно перетворювати ультрафіолетову частину сонячного світла у видиме світло. Цей процес є досить екологічним (це додаткові кольори червоного). Використання цього типу пластику для будівництва теплиць може дозволити рослинам поглинати більше видимого світла та збільшити врожайність приблизно на 10%.
Європій також можна застосовувати для квантових мікросхем пам'яті, які можуть надійно зберігати інформацію протягом кількох днів поспіль. Це дозволяє зберігати конфіденційні квантові дані в пристрої, подібному до жорсткого диска, та доставляти їх по всій країні.
Час публікації: 27 червня 2023 р.